Marta Burzyńska
Miód rzepakowy pod lupą
Miód rzepakowy jest pierwszym wiosennym miodem towarowym, pozyskiwanym przez pszczelarzy w maju. W formie płynnej charakteryzuje się jasną, kremowosłomkową barwą, a po szybkiej krystalizacji przybiera białą lub szarokremową. W konsystencji jest twardy, o kaszkowatej strukturze. Krupiec jest mało smarowny, dlatego bardzo popularne jest kremowanie miodów szybko krystalizujących, które stają się napowietrzone i lepsze w konsumpcji dzięki mazistej konsystencji.

Fot. Roman Dudzik
Badania przeprowadzone przez zespół badaczy Laboratorium Badania Jakości Produktów Pszczelich w Puławach w 2011 roku wykazały, że parametry fizykochemiczne miodu rzepakowego nie zmieniły się istotnie w ciągu ostatnich 30 lat pomimo wprowadzenia nowych odmian rzepaku w rolnictwie i wdrożenia nowoczesnych metod analitycznych w badaniach laboratoryjnych.
Charakterystyka pożytku
Miód rzepakowy jest jednym z najbardziej znanych nektarowych miodów odmianowych w Polsce. Pozyskiwany jest z kwiatów rzepaku (Brasicca napus L.), który kwitnie pod koniec kwietnia i na początku maja [Hołderna-Kędzia 2001]. Zarówno odmiany rzepaku ozimego, jak i jarego są szeroko rozpowszechnione i uznawane od lat w wielu krajach, zwłaszcza w Europie Środkowej i Wschodniej jako doskonała roślina paszowa dla pszczół.
Jej głównym przeznaczeniem jest produkcja oleju z nasion, a odpady poprodukcyjne z powodzeniem wykorzystywane są jako cenna pasza dla zwierząt (śruta poekstrakcyjna i słoma), ale także na cele energetyczne i w produkcji biodiesela. Dla większości pszczelarzy właśnie od miodu rzepakowego rozpoczyna się sezon pszczelarski. Wydajność miodowa rzepaku wynosi od 80–140 kg na ha w przypadku rzepaku ozimego i do 60-80 kg na ha dla rzepaku jarego i wydajność pyłkowa: 100–150 kg. Badania przeprowadzone w Chinach wykazały, że obnóża pyłkowe z rzepaku zawierają: 27,3% białka i 6,6% tłuszczu [Yang i in. 201]; podobne wyniki zostały opublikowane przez brazylijskich naukowców: 23–24,5% białka i 4,7–6,2% tłuszczu [Souza 2014].
Badania wskazują, że rzepak dostarcza nie tylko pokarmu węglowodanowego pszczołom, ale również jest dobrym źródłem białka i tłuszczu w diecie pszczoły miodnej. Jest to istotne szczególnie w kwietniu i maju, kiedy najbardziej potrzebne są związki budulcowe i wzmacniające rodzinę podczas wiosennego rozwoju. Niestety monokultury rzepaku w krajobrazie Polski powodują, że baza pożytkowa pszczół w okresie od kwietnia do maja jest coraz uboższa i pomimo dość dobrej wartości odżywczej pyłku rzepaku, niestety przez intensywność uprawy, prowadzi do monodiety i braku różnorodnych składników odżywczych z innych pożytków.
Cechy organoleptyczne
Miód rzepakowy ma charakterystyczny zapach kwiatów rzepaku. W smaku jest delikatny, bardzo słodki z odrobiną goryczki [Czerwińska 2009].
Tekstura
Miód rzepakowy należy do miodów najszybciej krystalizujących (od trzech dni do dwóch tygodni) ze względu na wyższą zawartość glukozy niż fruktozy. Krystalizuje drobnokrystalicznie, co sprawia wrażenie aksamitności [Cavia i in. 2002].
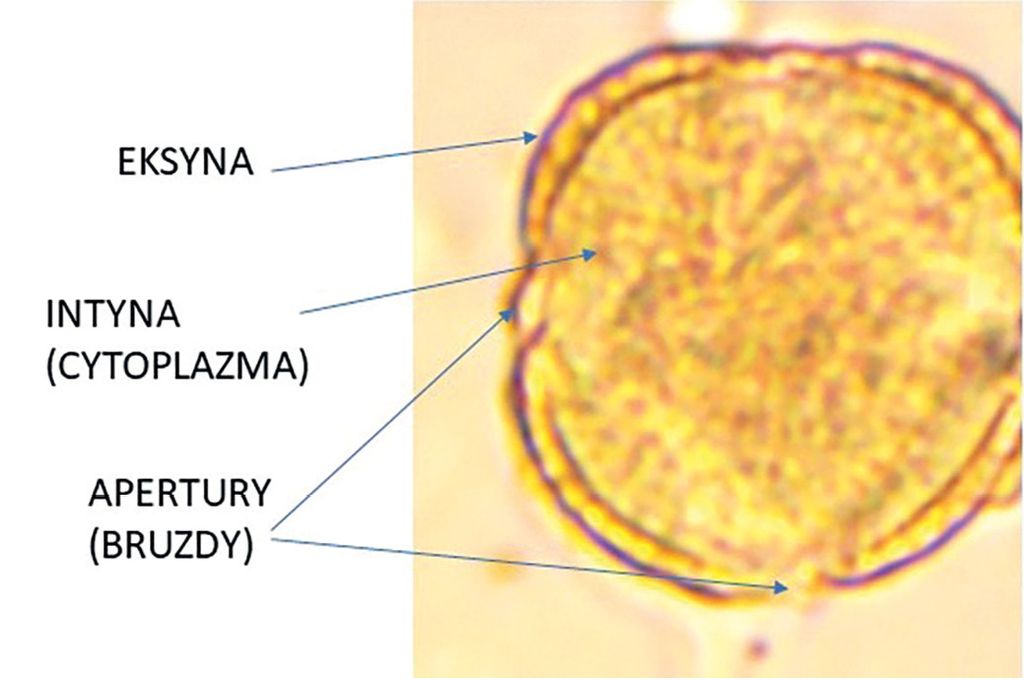
Fot. 1. Budowa ziarna pyłku rzepaku. Fot. Marta Burzyńska
Skład chemiczny
Miód rzepakowy zawiera 50-52% glukozy i 45-47% fruktozy. Zawartość pozostałych cukrów w miodzie jest marginalna: sacharoza 0,2–1,0%, maltoza do ok. 5% oraz niecałe 0,5% trójcukru melecytozy [Okniański 2006].
Ta odmiana, jak większość miodów wiosennych, ma niską zawartość wolnych kwasów, od 11 do 17 mval/kg, niską przewodność elektryczną, średnio 0,20 mS/cm, oraz najniższą zawartość wolnej proliny, ok. 18-24,1 mg/100 g. Niska aktywność enzymatyczna, co potwierdzają badania nad aktywnością α-amylazy, która jest wyrażana liczbą diastazową – DN (wg skali Schade), w miodach rzepakowych wynosi średnio 14,0 Schade [Persano Oddo i Piro, 2004, Szczęsna i in. 2011].
Kolejnym wyróżnikiem jakościowym dla miodów jest zawartość HMF. W badaniach Laboratorium Jakości Produktów Pszczelich w Puławach [2011], zawartość HMF wahała się od 0,5 do 13,1 mg/kg, natomiast w badaniach Śliwińskiej i wsp. [2012] określono ją na poziomie 27,3 mg/kg. Wyróżnik ten wskazuje na warunki, w jakich przechowywany jest miód. Im wyższa temperatura (np. podgrzewanie w celu upłynnienia), dostęp światła oraz im dłuższy czas magazynowania, tym wykładniczo wzrasta poziom tego niekorzystnego związku w miodzie. Zawartość wody jest zazwyczaj niższa, niż dopuszczają normatywne akty prawne (20%) i średnio wynosi 18%.
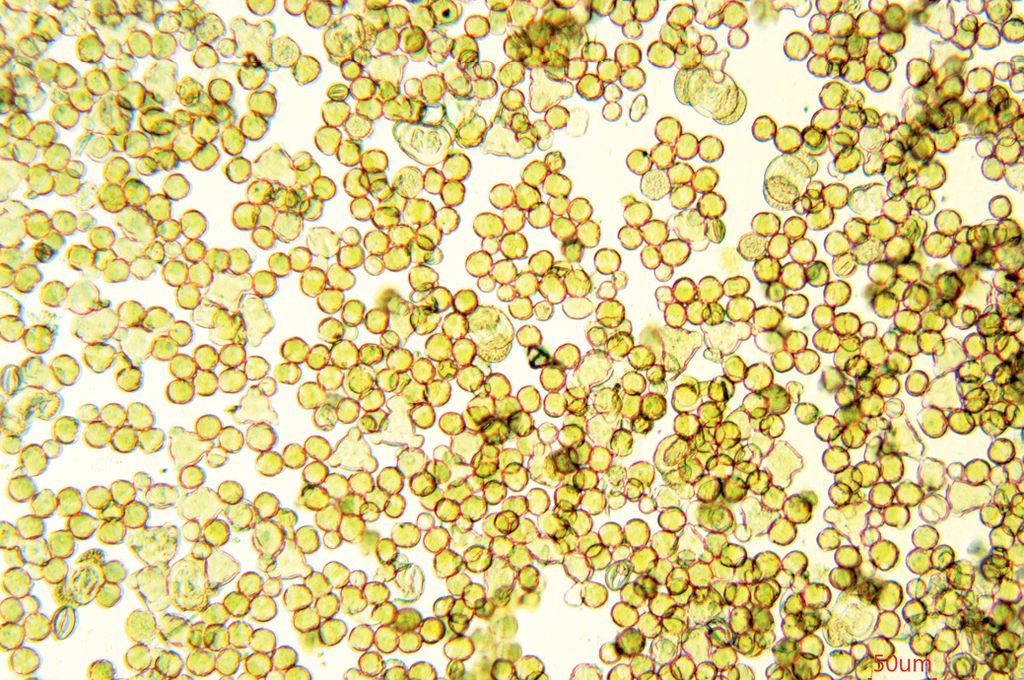
Fot. 2. Obraz mikroskopowy osadu miodowego (powiększenie 10x) typowy dla miodu rzepakowego. Fot. Marta Burzyńska
Miód rzepakowy zawiera olejki eteryczne, garbniki, związki goryczkowe, kwas nikotynowy, cholinę, kumarynę, saponiny, biopierwiastki, witaminy z grupy B, ale także witaminę K i C. Jest źródłem dobrze przyswajalnego żelaza oraz boru, który jest niezwykle cennym pierwiastkiem, zawiera również takie makroelementy jak wapń i magnez [Hołderna-Kędzia 2001]. Niestety bardzo często w miodach rzepakowych oznacza się metale ciężkie, szczególnie ołów [Chudzinska i Baralkiewicz 2010].
W miodach mogą kumulować się metale ciężkie, takie jak związki kadmu, miedzi, ołowiu, cynku i arsenu, co jest bezpośrednio związane z zanieczyszczeniem danego obszaru (najczęściej gleb i wód), na którym rosną rośliny miododajne. Pszczoły przenoszą do ula razem z surowcami roślinnymi i pobraną wodą także zanieczyszczenia pochodzące ze środowiska wynikające z emisji przemysłowych czy stosowania agrochemikaliów. Śladowe ilości pierwiastków toksycznych w miodach rzepakowych może mieć powiązanie z wieloletnią i coraz intensywniejszą chemizacją rolnictwa oraz związane z tym zwiększające się ilości oprysków na polach uprawnych [Munoz Olivas i Camara 2001; Wang i in. 2010].
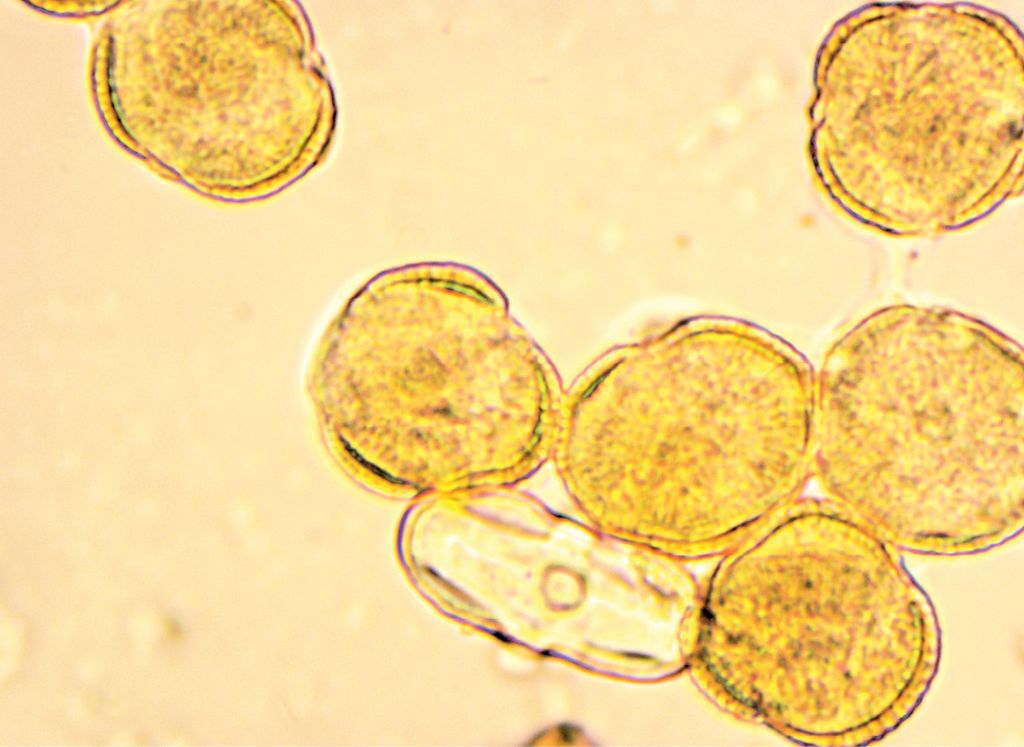
Fot. 3. Obraz mikroskopowy pyłku rzepaku przy powiększeniu 100x. Fot. Marta Burzyńska
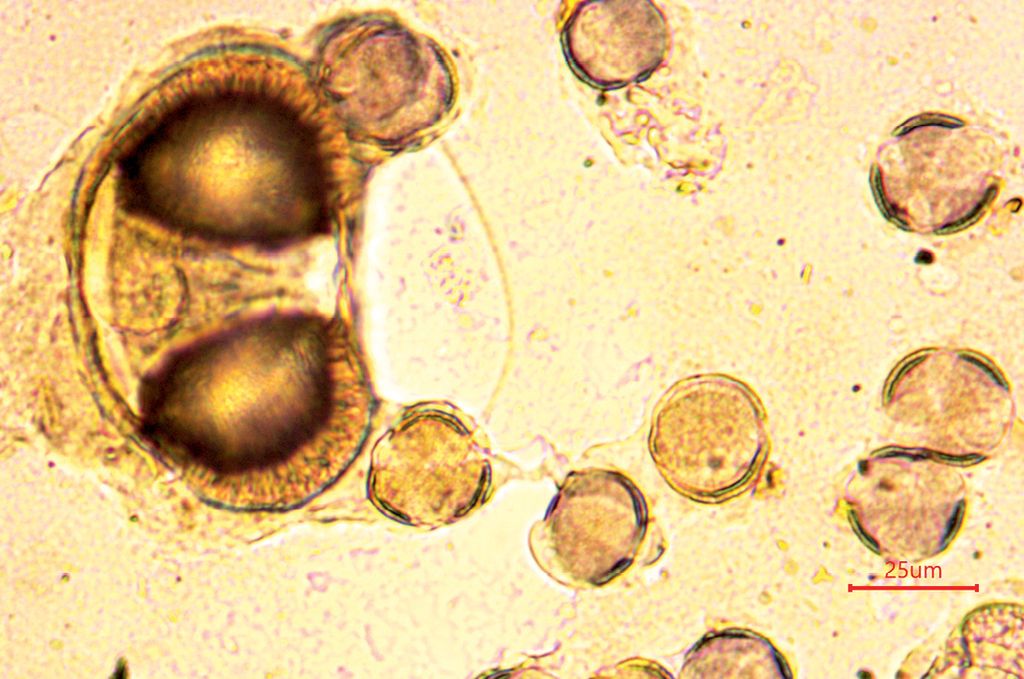
Fot. 4. Obraz mikroskopowy osadu miodu rzepakowego (powiększenie 100x) ukazujący różnice w wielkości pyłku rzepaku (rośliny owadopylnej) i sosny (rośliny wiatropylnej). Fot. Marta Burzyńska
Wymagania jakościowe (tabela)
Wymagania jakościowe dla miodów określa: Dyrektywa Parlamentu Europejskiego i Rady 2014/63/UE z dnia 15 maja 2014 r. zmieniająca dyrektywę Rady 2001/110/WE oraz na jej podstawie uchwalone Rozporządzenie Ministra Rolnictwa i Rozwoju Wsi z dnia 3 października 2003 r. w sprawie szczegółowych wymagań w zakresie jakości handlowej miodu (Dz.U. 2003.181.1773), którego wejście w życie uchyliło Polską Normę – Miód Pszczeli (PN-88/A-77626).
W ostatnich latach Międzynarodowa Komisja Miodowa (IHC – International Honey Commission) opracowała parametry fizykochemiczne dla 15 odmianowych miodów, które najczęściej pozyskuje się w Europie. Spośród wybranych miodów znalazł się również miód rzepakowy [Persano Oddo i Piro 2004]. W poniższej tabeli zebrane zostały szczegółowe wymagania w zakresie jakości handlowej polskich miodów rzepakowych:
|
Badana substancja |
Kryteria |
|
Zawartość wody |
nie więcej niż 20% |
|
Zawartość fruktozy i glukozy (suma fruktozy i glukozy) |
nie mniej niż 60 g/100 g |
|
Zawartość sacharozy |
nie więcej niż 5 g/100 g |
|
Zawartość substancji nierozpuszczalnych w wodzie |
nie więcej niż: 0,1 g/100 g |
|
Przewodność właściwa |
nie więcej niż 0,8 mS/cm |
|
Wolne kwasy |
nie więcej niż 50 mval/kg |
|
Liczba diastazowa |
nie mniej niż 8 |
|
Zawartość 5-hydroksymetylofurfuralu (HMF) |
nie więcej niż 40 mg/kg |
|
Zawartość proliny |
PN-88/A-77626 Miód pszczeli – 25 mg/100 g |
|
Analiza pyłkowa |
Rozporządzenia Ministra Rolnictwa i Rozwoju Wsi z dnia 14.01.2009 r. (Dz. U. Nr 17, poz. 94) pkt. VI i PN-88/A-77626 Miód pszczeli |
Tabela 1. Wymagania jakościowe dla miodu rzepakowego na podstawie Dz.U. z 2009 r. Nr 17 poz. 94 oraz PN-88/A-77626:1988
Budowa pyłku na przykładzie Brassica napus
W miodach znajduje się pyłek, na podstawie którego określa się odmianę miodu nektarowego. Ziarna pyłku mają najczęściej kształt kulisty lub elipsoidalny, ale także trójkątny, a ich wielkość jest bardzo zróżnicowana i wyrażana jest w mikrometrach (1 µm = 0,0001 mm). Poznane i zidentyfikowane w osadach miodowych zostały różne ziarna pyłków, od najmniejszych, zaledwie 3 µm (niezapominajka), do nawet 220 µm (dynia zwyczajna) Najczęściej ziarna pyłku mają ok. 25-50 µm średnicy [Podbielkowski 1982; Lack i Evans 2005].
Zawartość pyłku rzepaku w miodach rzepakowych
Udział pyłku rzepaku (Brassica napus) w tych odmianowych miodach nie może być niższy niż 45%. Określa to Polska Norma „Miód pszczeli” (PN–88/A–77626), która przestała obwiązywać w momencie wejścia w życie Rozporządzenia Ministra Rolnictwa i Rozwoju Wsi z dnia 3 października 2003 r. w sprawie szczegółowych wymagań w zakresie jakości handlowej miodu (Dz.U. 2003 nr 181 poz. 1773).
Dokument ten jednak nie zawiera informacji nt. procentowego udziału pyłku przewodniego w miodach odmianowych, dlatego Polska Norma (PN–88/A–77626) obowiązuje wciąż w części dotyczącej klasyfikacji miodów nektarowych do danej odmiany. W szczegółowych badaniach melisopanologicznych, wykonując ilościową analizę pyłkową, miody rzepakowe można zakwalifikować do II klasy, a więc miody te powinny zawierać 20-100 tys. ziaren w 10 g miodu.
Zawartość pyłku Brassica napus w przebadanych miodach rzepakowych (n=105) z całej Polski, przez Laboratorium Jakości Produktów Pszczelich w Puławach, wyniosła 45,2–66,8% (średnio 52,3%), a całkowita liczba ziaren pyłku w 10 g miodu (PG/10 g) mieściła się w granicach 18 500–61 100 (średnio 46 200) [Szczęsna i in. 2011].
Fotografia nr 2 przedstawia obraz mikroskopowy osadu miodowego (powiększenie 10x) typowy dla miodu rzepakowego, gdzie można zaobserwować znaczne zagęszczenie ziaren pyłku rzepaku i nieliczne pyłki o znaczeniu drugorzędnym. Zdjęcie nr 3 przedstawia obraz mikroskopowy pyłku rzepaku przy powiększeniu 100x. Fotografia nr 4 to obraz mikroskopowy osadu miodu rzepakowego (powiększenie 100x) ukazujący różnice w wielkości pyłku rzepaku (rośliny owadopylnej) i sosny (rośliny wiatropylnej).
Właściwości zdrowotne
Miody rzepakowe ze względu na niską aktywność enzymatyczną (niewielka zawartości α-amylazy), również małą ilość wolnych kwasów i niską przewodność właściwą, nie wykazują wysokiej aktywności biologicznej oraz antybiotycznej. Są miodami dość łagodnymi w smaku o neutralnym aromacie, co szczególnie odpowiada młodszym konsumentom. Ze względu na wysoką zawartość glukozy, zaleca się miód rzepakowy dla wzmocnienia serca oraz w profilaktyce choroby wieńcowej i ogólnie w chorobach układu krążenia. Przynosi korzyści w schorzeniach układu krwionośnego.
Zwiększa potencjał skurczu przeciążonego serca. Zapewnia lepsze dostarczanie tlenu i składników odżywczych do mięśnia sercowego. Również stosowany dla poprawy funkcjonowania wątroby, gdyż wywiera korzystny wpływ na przemiany tłuszczów w tym organie i poprawia funkcjonowanie pęcherzyka żółciowego. Lecznicze właściwości miodu rzepakowego wykorzystywane są również w stanach zapalnych dróg oddechowych. Osłabia kaszel i wspomaga odporność organizmu [Hołderna-Kędzia 2001].
W stanach osłabienia, przemęczenia i w okresach przeziębień jako środek wzmacniający, szczególnie polecany w postaci ciepłego roztworu wodnego. Ze względu na zawartości cukrów prostych, miód rzepakowy odżywia i regeneruje wyczerpany organizm, dodatkowo pomaga uzupełniać niedobory boru, wapnia i magnezu.
Również dlatego szczególnie polecany jest dla osób w wieku podeszłym. Z uwagi na obecność boru przyczynia się do prawidłowej budowy kości, pracy tarczycy i śledziony. Likwiduje nadmiar wody obecnej w tkankach i redukuje obrzęki spowodowane jej kumulacją, dzięki właściwościom osmotycznym. Reguluje ciśnienie tętnicze krwi i hamuje rozwój miażdżycy.
Usuwa z organizmu toksyczne produkty przemiany materii w wyniku wiązania ich z kwasem glukuronowym (wytwarzanym z glukozy) i flawonoidami. Zalecany jest w dolegliwościach związanych z zaburzonym funkcjonowaniem nerek i układu moczowego. Ponadto usprawnia gojenie stanów zapalnych żołądka i dwunastnicy w chorobie wrzodowej [Baczmiański i Gruszczyński 2008].
Z drugiej strony należy pamiętać, że miód to w 80% cukier i w większych dawkach może powodować zaburzenia w gospodarce glukozy, szczególnie u osób obciążonych chorobami przewlekłymi, takimi jak hiperglikemia, hipoglikemia oraz insulinooporność. Dlatego ważne jest, aby wykorzystując miód w lecznictwie, zawsze zaczynać od niewielkich dawek i bacznie obserwować reakcję organizmu na zachodzące zmiany. W razie braku skutków ubocznych dawkę można zwiększać, aż do uzyskania zadowalającego efektu.
mgr inż. Marta Burzyńska
Katedra Biochemii i Analizy Żywności
Wydział Nauk o Żywności i Żywieniu
Uniwersytet Przyrodniczy w Poznaniu
Literatura
Baczmiański J, Gruszczyński R. Miód to zdrowie. Ekonatura 2008;10, s. 8-9.
Cavia M.M., Fernández-Muiño M.A., Gömez-Alonso E., Montes-Pérez M.J., Huidobro J.F. & Sancho M.T. 2002. Evolution of fructose and glucose in honey over one year: influence of induced granulation. Food Chemistry 78(2). s. 157-161.
Chudzinska, M., & Baralkiewicz, D. (2010). Estimation of honey authenticity by multielements characteristics using inductively coupled plasma-mass spectrometry (ICP-MS) combined with chemometrics. Food and Chemical Toxicology, 48, s. 284–290.
Czerwińska D. Miodowy miesiąc. Przegl Gastron 2009;63(12), s. 6-7.
Dyrektywa Parlamentu Europejskiego i Rady 2014/63/UE z dnia 15 maja 2014r.
Hołderna-Kędzia E. Charakterystyka miodu rzepakowego. Pszczelarstwo 2001;52(4), s.7.
Karpowicz W.,: Z ewolucji roślin. Warszawa: Państwowe Zakłady Wydawnictw Szkolnych, 1972, s. 12-13.
Lack A.J., Evans D.E.: Biologia roślin. Krótkie wykłady. Warszawa: Wydawnictwo Naukowe PWN, 2005. ISBN 83-01-14006-2.
Munoz Olivas R., Camara C., Speciation related to human health. w: Ebdon L., Pitts L., Cornelis R., Crew H., Donard O.F.X., Quevauviller P., Trace element speciation for environment, food and health. UK: The Royal Society of Chemistry; 2001. s. 33-53.
Okniański P. Polskie płynne złoto. Miody odmianowe. Pasieka 2006; s. 14-7.
Persano Oddo L., Piro R. Main European unifloral honeys: descriptive sheets. Apidologie, 35: (2004), s. 38-81.
PN-88/A-77626 „Miód pszczeli”
Podbielkowski Z.: Rozmnażanie się roślin. Warszawa: Wydawnictwa Szkolne i Pedagogiczne, 1982, s. 235. ISBN 83-02-01456-7.
Rozporządzenie Ministra Rolnictwa i Rozwoju Wsi z dnia 3 października 2003 r. w sprawie szczegółowych wymagań w zakresie jakości handlowej miodu (Dz. U. Nr 181, poz. 1773, z późn. zm.).
Rozporządzeniem Ministra Rolnictwa i Rozwoju Wsi z dnia 14 stycznia 2009 r. w sprawie metod analiz związanych z dokonaniem oceny miodu (Dz. U. Nr 17, poz. 94).
Souza BR (2014) Quantificação das vitaminas do complexo B (B1, B2) e vitâmeros das vitaminas B3 e B6 em amostras de pólen apícola desidratado provenientes da Região Sul do Brasil.
Szczesna T., Rybak-Chmielewska H., Waś E., Kachaniuk K., Teper D. (2011). Characteristics of Polish unifloral honeys. I. Rape honey (Brassica napus L. Var. oleifera Metzger). Journal of Apicultural Science. 55. S.111-119.
Śliwińska A., Przybylska A., Bazylak G., Wpływ zmian temperatury przechowywania na zawartość 5-hydroksymetylofurfuralu w odmianowych i wielokwiatowych miodach pszczelich, Bromat. Chem. Toksykol. – XLV, 2012, 3, s. 271–279
Wang J., Kliks M.M., Jun S., Li Q.X., Residues of organochlorine pesticides in honeys from different geographic regions. Food Research International, 43, 2010, s. 2329–2334.
Wilczyńska A., Rój A., Przybyłowski P., Próba identyfikacji związków fenolowych w miodach pszczelich, Brom. i Chem. Toksykol., suplement, 2005, s. 197–201.
Yang K, Wu D, Ye X, Liu D, Chen J, Sun P (2013) Characterization of chemical composition of bee pollen in China. J Agric Food Chem 61, s. 708–718





